A、常温下,1L0.1mol·L-1的NH4NO3溶液中氮原子数小于0.2×6.02×1023
B、用100mL4mol·L-1盐酸与8.7gMnO2共热能制取氯气分子数为0.1×6.02×1023
C、0.1mol8135Br原子中含中子数为3.5×6.02×1023
D、用粗铜作阳极电解稀硫酸,当生成0.1molH2时,阳极失去的电子数为0.2×6.02×1023
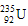 核素,含有235×6.02×1023个中子
核素,含有235×6.02×1023个中子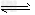 2NH3(g)ΔH=-92.4kJ/mol可知每断开6NA个N-H键所释放热量小于92.4kJ
2NH3(g)ΔH=-92.4kJ/mol可知每断开6NA个N-H键所释放热量小于92.4kJ