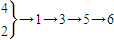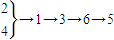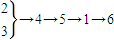试题检索 :
教材版本 :
课本 :
题型 :
难易度 :
NH4 NO3 俗名硝铵,是一种重要的化学炸药,也广泛用于农业施肥.工业上以空气、煤等原料制NH4 NO3 .生产过程为①生成氨②空气液化分离③氨氧化④制水煤气⑤生成HNO3 ⑥生成NH4 NO3 则最合理的流程为( )
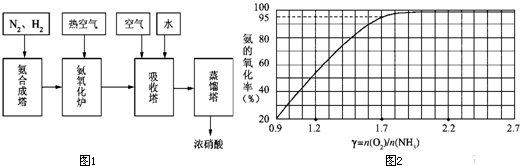
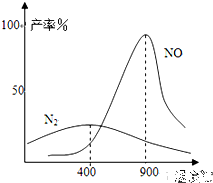
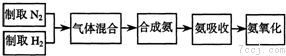
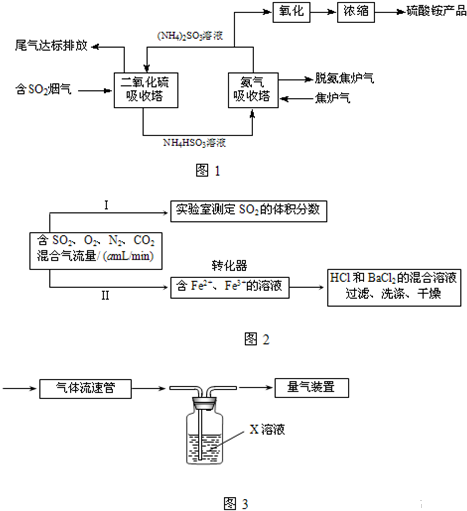
工业合成氨与制备硝酸一般可连续生产,流程如图1:2 O.在实际生产中氨的氧化率与混合气中氧氨比(氧气与氨气物质的量比,以γ{n(O2 )/n(NH3 )}表示)的关系如图2所示.2 )/n (NH3 )}为1.25,而实际生产要将γ值维持在1.7~2.2之间,其原因是______.3 和足量空气为原料(不考虑N2 的反应)最大程度制取NH4 NO3 ,经过一系列转化反应后,向反应后的混合物中加入b g水,得到密度为ρ g•mL-1 的溶液,计算该溶液中NH4 NO3 物质的量浓度可能的最大值______.
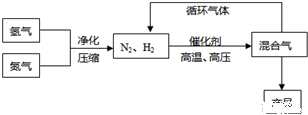
工业上合成氨是在一定条件下进行如下反应:2 (g)+3H2 (g)⇌2NH3 (g),△H=-92.44kJ/mol;其部分工艺流程如下:气体 氮气 氢气 氨 熔点(℃) -210.01 -252.77 -77.74 沸点(℃) -195.79 -259.23 -33.42
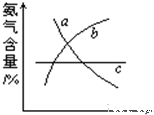
回答下列问题:2 的转化率越高 B.NH3 的产率越大2 的含量越高 D.化学反应速率越快
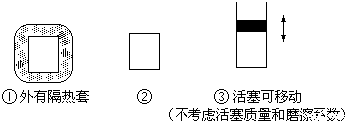
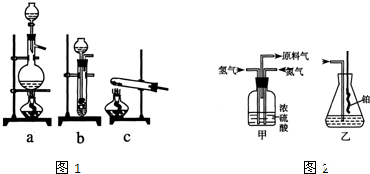
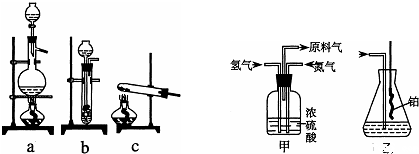
实验室模拟合成氨和氨催化氧化的流程如下:2 )溶液与饱和氯化铵溶液经加热后反应制取氮气. 、氢气 、 (“会”或“不会”)发生倒吸,原因是: . + 、OH- 、 、 离子.
我国硫酸工业年SO2 排放量约10万吨,硫酸工业的尾气必须进行处理. ;设计一个简单的实验方案,检验尾气中是否含有氨气: . .3+ 的氧化性,将SO2 氧化成SO4 2- 而实现SO2 的回收利用.2 的体积分数.X溶液可以选用 .2 的体积分数,取280mL(标准状况)气体样品与足量Fe2 (SO4 )3 溶液完全反应后,用浓度为0.020mol/L的K2 Cr2 O7 溶液滴定反应生成的Fe2+ ,至终点消耗K2 Cr2 O7 溶液25.00mL.尾气中SO2 的体积分数为 .2 O7 2- +Fe2+ +H+ →Cr3+ +Fe3+ +H2 O(未配平)2 氧化成SO4 2- 的转化率,该实验中还需测定的数据有 、 .
(1)工业上合成氨的反应方程式为 ,反应是在 中进行,该设备的出口处的气体是 (填写分子式). 种. (填增大、减小、不变).+ 的物质的量浓度为 mol/L. 12(填<、>、=).
氮元素在生命活动中扮演着十分重要的角色,回答下列与氮及其化合物有关的问题.3
实验室模拟合成氨和氨催化氧化的流程如下:2 )溶液与饱和氯化铵溶液经加热后反应制取氮气.2 B NO2 C HNO3 D NH4 NO3 2 O
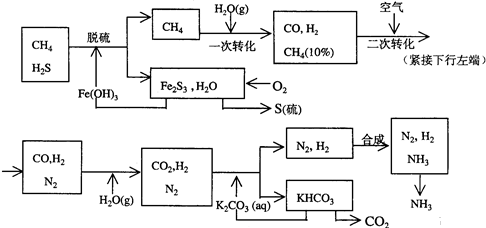
利用天然气合成氨的工艺流程示意如下:4 经一次转化后产生CO 0.9n mol、产生H2 ______mol(用含n的代数式表示)2 CO3 (aq)和 CO2 反应在加压下进行,加压的理论依据是______(多选扣分)3 分解得到的CO2 可以用于______(写出CO2 的一种重要用途).3 循环,二是K2 CO3 (aq)循环,请在上述流程图中标出第三处循环(循环方向、循环物质)
本站特点
1. 致力于在线题库开发
2. 提供优质的组卷服务
商务联系
手机/微信 : 15036480330
手机/微信 : 13474117172
QQ : 416148514