作者 : qq_巷篱三木樟 ·
收藏试卷 显示答案 下载试卷 纯净版 全部添加至试题篮
 气成分相似③火星上钢铁不容易生锈 ④火星环境适宜人类生存⑤火星上温室效应显著。你认为正确的是
气成分相似③火星上钢铁不容易生锈 ④火星环境适宜人类生存⑤火星上温室效应显著。你认为正确的是 | 实验目的 | 所加试剂 (或操作、图示) | 实验现象 | 实验结论 | |
| A | 检验稀盐酸和氢氧化钠溶液是否恰好完全反应 | 在反应后的溶液中滴加无色酚酞试液 | 无明显现象 | 恰好完全反应 |
| B | 判断海水和蒸馏水 | 蒸发结晶 | 液体消失,无残留物 | 该液体为蒸馏水 |
| C | 检验溶液中是否含硫酸根离子 | 加入氯化钡溶液,再加入稀硝酸 | 有白色沉淀产生 | 溶液中一定含硫酸根离子 |
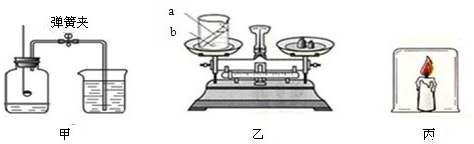
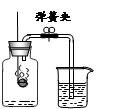
| D | 测定空气中氧气的体积分数 | 完全燃烧后,冷却至室温,打开弹簧夹,进入水的体积约为集气瓶总体积的五分之一 | 氧气约占空气体积的五分之一 |

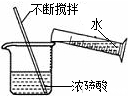 稀释浓硫酸
稀释浓硫酸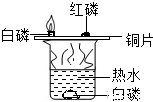 探究燃烧的三个条件
探究燃烧的三个条件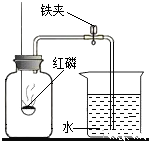 测定空气中氧气的含量
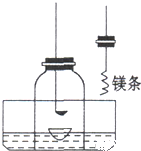
测定空气中氧气的含量 验证质量守恒定律
验证质量守恒定律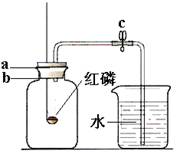
| 第一组 | 第二组 | 第三组 | |||||||||
| 集气瓶编号 | ① | ② | ③ | ④ | ⑤ | ① | ② | ③ | ④ | ⑤ | ① |
| 收集的O2占容积的体积分数(%) | l0 | 20 | 30 | 40 | 50 | 3l | 33 | 35 | 37 | 39 | 34 |
| 带火星木条的状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 | 很亮 | 很亮 | 复燃 | 复燃 | 复燃 | 很亮 |