CO+H2;②CO+H2O(g)
CO+H2;②CO+H2O(g) CO2+H2;
CO2+H2; O2(g)═CO2(g)△H=-283.0KJ/mol;
O2(g)═CO2(g)△H=-283.0KJ/mol; O2(g)=H2O(g)△H=-285.8KJ/mol;
O2(g)=H2O(g)△H=-285.8KJ/mol;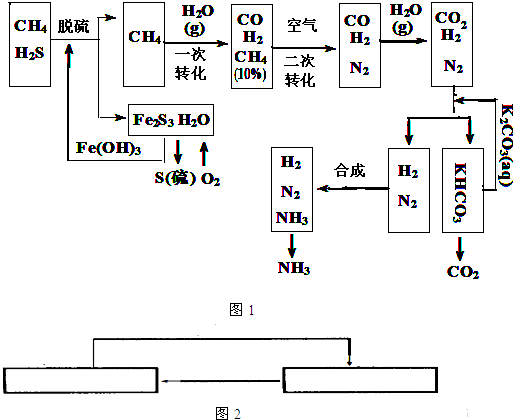
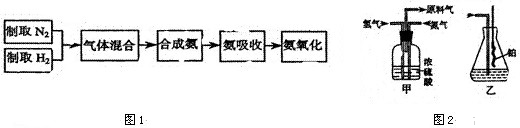
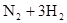

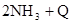 下列说法正确的是( )
下列说法正确的是( )  ,当重新达到平衡时,
,当重新达到平衡时,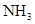 的平衡浓度比原平衡时增大,
的平衡浓度比原平衡时增大,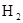 的浓度比原平衡时减少(反应前后体积不变)。
的浓度比原平衡时减少(反应前后体积不变)。 ,当重新达到平衡时,
,当重新达到平衡时, 在混合气中体积分数增大。
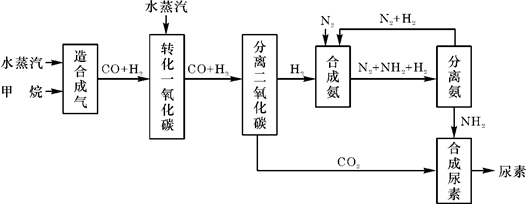
在混合气中体积分数增大。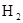 可由煤与水反应制得,其中有一步反应为
可由煤与水反应制得,其中有一步反应为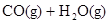

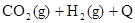 ,欲提高
,欲提高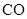 转化率可采用的方法是()
转化率可采用的方法是()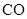 浓度;⑤增大水蒸气浓度
浓度;⑤增大水蒸气浓度 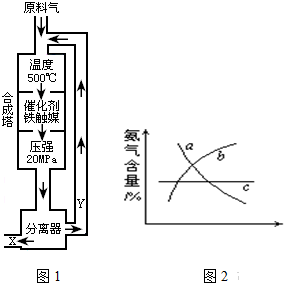
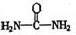 ,请写出两种含有碳氧双键的尿素的同分异构体的结构简式:① ,② 。
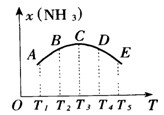
,请写出两种含有碳氧双键的尿素的同分异构体的结构简式:① ,② 。  2NH3,并分别在t0秒时测定其中NH3的体积分数[x(NH3)],绘成如图的曲线。
2NH3,并分别在t0秒时测定其中NH3的体积分数[x(NH3)],绘成如图的曲线。