-
试题检索 :
-
教材版本 :
-
课本 :
-
题型 :
-
难易度 :
已知空气的主要成分是氮气和氧气,某课外活动小组设计测定空气中氧气含量的实验,实验装置如图所示:
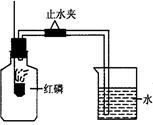
⑴红磷燃烧的现象 ,
红磷在集气瓶中发生反应的文字表达式为 。
该实验中红磷稍过量,目的是 。
⑵待燃烧停止,白烟消失并冷却后,打开止水夹,观察到烧杯中的水进入集气瓶,瓶内水量约占 ,由本实验还可以推知氮气的哪一性质?试写出其中一种 。
⑶若将红磷换成炭粉,该实验能否获得成功? ,理由是
用如图装置测定空气中氧气含量.将燃烧匙内红磷点燃迅速伸入广口瓶并塞上胶塞.
(1)红磷燃烧的主要现象是 ,反应的文字表达式为 .
(2)燃烧停止,白烟消失后,广口瓶内水面上升约 体积,由此说明空气中氧气约占 体积.
(3)实验结束后,拔开胶塞,迅速伸入一燃着的木条,请猜测可能发生的现象 .
(4)若实验结果氧气的含量还不到20%,分析造成这种结果可能的原因有:
① ;
② ;
③ .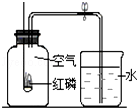
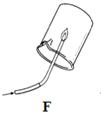
气体的密度容易受温度和压强的影响.为了测量常温常压下氧气的密度,在老师的指导下,小明进行了如下实验:
步骤一:检查发生装置的气密性.
步骤二:往烧瓶中装入适量的二氧化锰粉未.关闭分液漏斗的活塞,并将适童的过氧化氢溶液倒人分液漏斗中,测出发生装置的总质量为m1克.
步骤三:取一个集气瓶,用记号笔在适当位置做标记,将水注入集气瓶到标记处,用量筒测出这些水的体积为V0毫升.再将集气瓶灌满水倒扣在水槽中等待收集.
步骤四:打开活塞,滴入过氧化氢溶液,同时干始收集气休.调节集气瓶在水中的上下位置,当集气瓶内、外的液面相平且刚好达到标记处时(如图).暂停反应.
步骤五:重复步骤四,再收集9瓶气体.
步骤六:称出反应后发生装置的总质量为m2克.
(1)小明通过该实验,测得氧气的密度是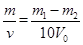 克/毫升.
克/毫升.
(2)步骤四中,控制集气瓶内、外液而保持相平的目的是 .
(3)如果实验中装置气密性不良,将对测得的密度值有何影响?请说明理由.
人类的生存离不开氧气。某校化学兴趣小组的同学在老师的指导下做了有关氧气的系列探究实验。


探究一:某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究。
⑴如右图所示装置和药品进行实验,反应的化学式表达式是: 。
⑵小明同学认为可用铁丝代替红磷测定空气中氧气的含量,小丽同学认为不可以,其原因是:
。
(3)小芳同学用木炭代替红磷来测定空气中氧气的含量。结果却发现水几乎没有倒吸。小组内同学帮她仔细检查,发现装置的气密性及操作步骤均无问题。你认为造成此现象的原因是 。
(4)小组内同学反思上述实验的探究过程后认为:用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是: 。
探究二:以下是该小组探究影响H2O2溶液反应速率部分因素的相关实验数据。
实验序号
| H2O2溶液浓度%
| H2O2溶液体积/mL
| 温度/℃
| MnO2的用量/g
| 收集氧气的体积/mL
| 反应所需
的时间/s
|
①
| 5
| 1
| 20
| 0.1
| 4
| 16 .75
|
②
| 15
| 1
| 20
| 0.1
| 4
| 6.04
|
③
| 30
| 5
| 35
| 0
| 2
| 49.21
|
④
| 30
| 5
| 55
| 0
| 2
| 10.76
|
⑴写出实验室用H2O2溶液和MnO2混合制氧气的化学式表达式:_________________。
⑵通过实验①和②对比可知,化学反应速率与____________有关;
从实验③和④对比可知,化学反应速率与温度的关系是:______________________。
⑶通过上述实验____(填“能”或“不能”)说明使用MnO2可以加快H2O2溶液反应速率。
如下图所示装置先在集气瓶里加少量水,再把剩余的容积用记号划分成 5等分。
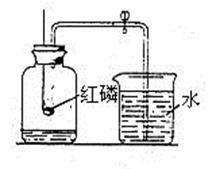
(1)点燃燃烧匙内的红磷,立即盖紧瓶塞,观察现象 。
火焰熄灭后,振荡集气瓶,装置冷却后,打开导管上的夹子,出现了什么现象 ;
消耗的气体跟剩下的气体的体积比约为 。
(2)实验说明: 。
(3)请推测集气瓶中剩余气体有哪些性质: (只写一条)。
(4)小明做完试验后发现得到的数据小于1/5,请你帮他分析一下可能的原因
(只写一条)
下图是小明同学用来验证空气中氧气体积含量的装置图。
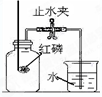
⑴ 磷燃烧时的主要实验现象是 。该反应的化学式表达式为 。
⑵小明打开止水夹后,发现进入广口瓶中的水达不到广口瓶容积的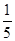 ,请你帮助他分析造成实验失败的可能原因是 。(写一条即可)
,请你帮助他分析造成实验失败的可能原因是 。(写一条即可)
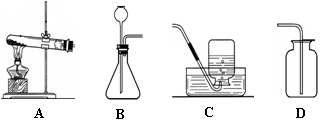
化学实验是学习化学的基础,请根据下列装置图回答问题。
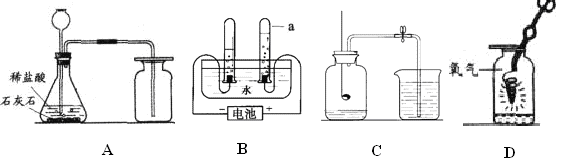
(1) B装置中a的仪器名称 。
(2) A装置中产生气体的化学方程式为 ,A装置还可以制取的气体是 。
(3) B装置反应的化学方程式为 。
(4)用C装置可做的实验名称是 。
(5)铁在氧气中反应的化学方程式为 _。
(6)按D装置实验时,集气瓶炸裂了,其可能的原因是 _。
化学是一门以实验为基础的科学,实验是学习化学的一条重要途径。根据以下实验解答下列问题:
⑴ 右图是测定空气中氧气含量的实验装置。实验中能得出“氧气约占空气总体积五分之一”结论的实验现象是 。

⑵ 若装置的气密性良好,去掉烧杯,点燃红磷,在装置完全冷却后,打开弹簧夹,装置的总质量会 (填“增加”、“减少”或“不变”)原因是 。
某化学兴趣小组的同学对教材中“测定空气里氧气含量”的实验做了改进,在密闭容器里进行磷的燃烧,以防止产生的白烟污染空气。他们设计了图示实验:选用容积为50 mL的试管作反应容器,选用50mL的注射器(开始时活塞处于20 mL刻度处)来测量磷燃烧时所消耗氧气的体积。
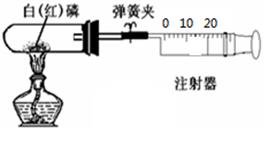
I.实验操作步骤如下:
(1)检查装置的气密性。
(2)装入药品,连接好仪器。
(3)夹紧弹簧夹,加热白磷,观察现象。
(4)等燃烧结束,试管冷却后打开弹簧夹,观察现象。
II.实验现象记录:
在步骤(3)中加热时观察到白磷燃烧,产生 ,此时活塞 移动(填“向左”或“向右”或“不”)。
在步骤(4)中待装置冷却后,打开弹簧夹,观察到活塞慢慢 移动(填“向左”或“向右”),最终停在约 mL刻度处(取整数值)。
Ⅲ.实验结论:氧气占空气的体积分数约为 。



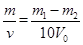 克/毫升.
克/毫升.



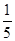 ,请你帮助他分析造成实验失败的可能原因是 。(写一条即可)
,请你帮助他分析造成实验失败的可能原因是 。(写一条即可) 

