 2(t-BuNO).
2(t-BuNO).
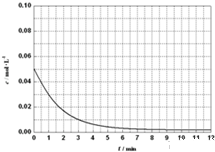
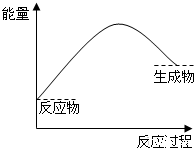
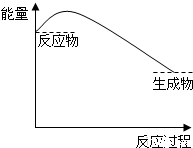
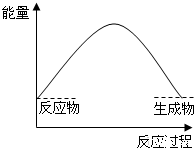
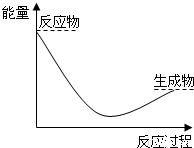
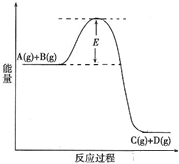 已知A(g)+B(g)⇌C(g)+D(g) 反应过程中的能量变化如图所示,回答下列问题.
已知A(g)+B(g)⇌C(g)+D(g) 反应过程中的能量变化如图所示,回答下列问题.
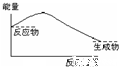
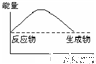

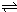 CH3OH(g)进行过程中的能量变化曲线.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.下列相关说法正确的是( )
CH3OH(g)进行过程中的能量变化曲线.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.下列相关说法正确的是( )
 CH3OH(g)△H=-91kJ•mol-1
CH3OH(g)△H=-91kJ•mol-1
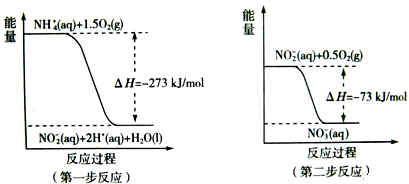
 2NH3(1)△H=-2(b+c-a)kJ•mol-1,其能量变化如图A所示
2NH3(1)△H=-2(b+c-a)kJ•mol-1,其能量变化如图A所示 2HI(g)△H<0,氢气的百分含量随温度和压强变化如图C所示
2HI(g)△H<0,氢气的百分含量随温度和压强变化如图C所示
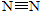 :946.5KJ/mol;N-H:391.0KJ/mol;则H-H键能为______.
:946.5KJ/mol;N-H:391.0KJ/mol;则H-H键能为______.| 物质 | △H(KJ/mol) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |