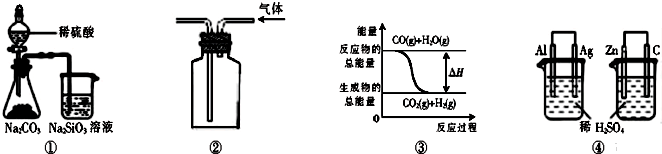
A、图①表示25℃时,用0.1 mol•L-1盐酸滴定20 mL 0.1 mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化
B、图②中曲线表示反应2SO2(g)+O2(g)⇌2SO3(g)+Q(Q>0)正、逆反应的平衡常数K随温度的变化
C、图③表示10 mL 0.01 mol•L-1 KMnO4 酸性溶液与过量的0.1 mol•L-1 H2C2O4溶液混合时(Mn2+是该反应的催化剂),n(Mn2+) 随时间的变化
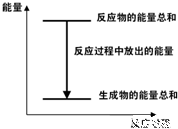
D、图④中a、b曲线分别表示反应CH2=CH2 (g)+H2(g)→CH3CH3(g)+Q(Q>0),使用和未使用催化剂时,反应过程中的能量变化